Détermination de la balance Hydrophile-Lipophile (HLB)
L'efficacité d'un émulsifiant est avant tout lié à sa solubilité dans chacune des deux phases. La solubilité de tout agent tensio-actif est caractérisée par sa balance hydrophile-lipophile (HLB). La phase dans laquelle l'émulsifiant sera le plus soluble formera la phase continue de l'émulsion. Un émulsifiant soluble dans l'eau stabilisera une émulsion huile dans eau et inversement. Les valeurs de la HLB s'échelonne entre 1 et 40 et, plus la HLB est élevée plus l'émulsifiant est hydrophile. La définition de la valeur de la HLB peut être réalisée de différentes manières.
Explication
On a pu mettre en évidence que pour un émulsifiant constitué par un ester d'acide gras et d'alcool polyhydroxylé il est possible d'atteindre la valeur de la HLB par la relation suivante (formule de Griffin):
HLB = 20 (1- S/A)
S représente l'indice de saponification de l'acide gras et A représente l'indice d'acide. Dans ces conditions, la HLB varie entre 0 totalement hydrophobe et 20 entièrement hydrophile. Ainsi pour le monostéarate de glycérol (1stéaryl sn glycérol) la HLB sera de 4,2 en sachant que l'indice de saponification est de 154,4 et l'indice d'acide de 197,1
HLB = 20 ( 1- 154,4/197,1) = 20 (1-0,79) = 4,2
La valeur est caractéristique d'une molécule hydrophobe qui sera utilisée pour stabiliser une émulsion eau dans huile.
Quand l'indice de saponification est difficile à obtenir, on utilise une autre relation qui est :
HLB = (E + P)/5
E représente le pourcentage de fonction oxyéthylénique, P représente le pourcentage d'alcool polyhydroxylé.
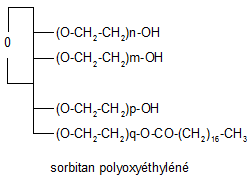
Dans le cas d'un sorbitol polyoxyéthylénique comme représenté dans la figure ci-dessus, si les valeurs de n,m, p et q sont identiques et égales à l' unité, E est estimé à 29% et P à 8%. La HLB est éqivalente à 7,4:
HLB = (29 + 8)/5 = 7,4
La valeur de la HLB préconiserait d'utiliser cet émulsifiant pour stabiliser une émulsion eau dans huile. Si les valeurs de n, m, p et q augmentent cela entraînera l'augmentation de la valeur de E et en conséquence celle de la HLB. En modulant l'éthérification on pourra obtenir des dérivés couvrant à la fois les valeurs hydrophobes et hydrophiles.
Une autre méthode est utilisable pour le calcul de la HLB, elle prend en compte les masses moléculaires des parties hydrophiles et la masse moléculaire de l'ester.
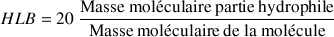
Ainsi pour l'ester suivant : CH3-(CH2)10-CO-O-(O-CH2-CH2)8-H la HLB sera équivalente à 13
car
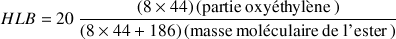
Enfin il est possible de définir et d'affecter à chaque groupement fonctionnel la valeur de l'énergie libre de transfert des groupes lipophiles et hydrophiles de l'émulsifiant au niveau de l'interface.
Davies et Lin ont effectué ces calculs, ils sont résumés dans le tableau suivant :
Voir tableau :
Explication
Ce qui permet de calculer la HLB comme étant :
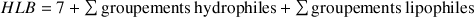
Ainsi pour un oléate de sodium on pourra définir :
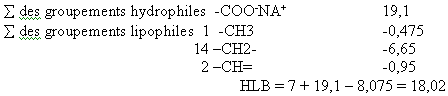
Toutes les valeurs affectées aux groupements ne font pas l'unanimité de la classe scientifique et il faut noter aussi que certains groupements n'ont pas été quantifiés, cependant cela reste une façon aisée de déterminer la HLB d'un émulsifiant.
Quand on utilise un mélange d'émulsifiant les valeurs de HLB sont additives. Le concept de la HLB est intéressant quand on veut comparer la qualité des émulsions et les propriétés stabilisatrices des émulsifiants. Cependant ce concept souffre de certaines insuffisances :
un émulsifiant commercial est généralement un mélange de molécules
la HLB ne prend pas en considération certains facteurs comme : l'ionisation en fonction du pH, l'influence de la température, la concentration en émulsifiant, l'interaction possible avec d'autres molécules et enfin la concentration respective des phases continues et dispersées.






