Introduction
Définition :
L'interestérification de la matière grasse peut s'approcher par le biais de 4 types différents de réaction : l'acidolyse, l'alcoolyse, la glycérolyse et la transestérification. La réaction résulte dans un premier temps d'une activation catalytique suivie de la coupure de la liaison ester et enfin échange des acides gras.
Explication
La réaction peut se faire sans catalyseur mais seulement à des températures élevées de l'ordre de 200°C pendant une période longue ce qui entraîne des dégradations des molécules sous l'action de la température. Les catalyseurs utilisés sont du type, base, acide et leurs sels correspondants. A haute température, les catalyseurs sont les sels métalliques de Cl-, CO3 -, NO3, Zn2+, Pb2+, Fe2+,Co2+, NaOH, LiOH. A basse température se sont préférentiellement des alkylates : méthylate ou éthylate de sodium ou de potassium. Les alkylates sont plus faciles à utiliser car ils agissent à des températures de l'ordre de 50°C voire inférieures et à des concentrations faibles de l'ordre de 0,1%. Si la concentration est supérieure, il y a possibilité de former des savons entraînant une diminution du rendement. L'aw du milieu est importante, il faut moins de 0,01% d'eau sinon les dérivés alkylés sont transformés en alcool et en savon. La teneur en acide gras libre ne doit pas dépasser 0,1% et la teneur en peroxyde doit être inférieure à 1%. La réaction est généralement arrêtée soit par addition d'eau soit par action d'un acide dilué.
Le mécanisme chimique est complètement aléatoire cependant on peut essayer de diriger la réaction d'interestérification
soit par le choix du catalyseur comme par exemple avec le méthoxylate de sodium qui permet un échange deux fois plus rapide en sn1,3 par rapport à sn2 après 24 heures de réaction. Ceci est vérifié dans le cas d'un échange entre la matière grasse du soja en présence de méthylstéarate,
soit par le choix des conditions expérimentales : il suffit de travailler à une température inférieure à celle du produit ayant le plus haut point de fusion (généralement un triacylglycérol saturé). Ainsi au fur et à mesure que le produit cristallise, il y a réarrangement des équilibres et on peut, de cette manière obtenir le maximum de produits saturé. Avec l'huile de coton qui renferme 24% d'acides gras saturés on peut obtenir par interestérification dirigée 19% de triacylglycérols saturés contre 1,5% si la réaction n'est pas dirigée.
Remarque
L'interestérification chimique est utilisée pour produire des graisses et des huiles qui serviront à la fabrication des margarines, des matières grasses culinaires. Le produit qui a été le plus étudié est le lard qui ne possède pas intrinsèquement de bonnes propriétés plastiques car il présente une apparence granuleuse, un aspect non attractif, une faible capacité au crémage, une mauvaise tenue en échangeur à surface raclée. On peut pallier à ces inconvénients en ajoutant un agent plastifiant mais on obtient par la suite, au stockage, un aspect de grain qui est du à la présence en sn2 d'un résidu de palmitate (64%). Par interestérification on obtient une diminution de 50% du taux de solide à 20°C, une augmentation de la plasticité et on empêche une texture graineuse. Le taux de palmitate en sn2 passe de 64% à 24%. Dans le cas des margarines, l'interestérification n'entraîne pas d'augmentation des acides gras insaturés trans comme c'est le cas par hydrogénation catalytique.
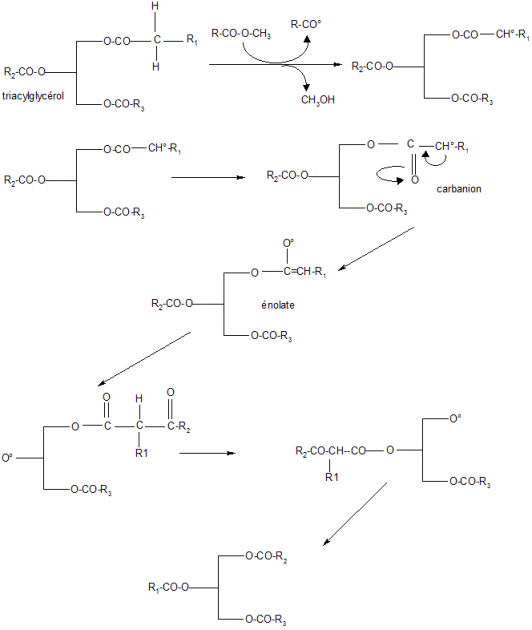
Deux mécanismes peuvent être évoqués pour expliquer cette réaction. Il y a la voie de la formation d'un énolate. Un ion énolate typique de l'action d'une base sur un ester est formé. L'ion énolate réagit avec une autre fonction ester pour produire un
 cetoester qui donnera le nouveau produit estérifié. Le mécanisme est évoqué dans la figure ci-dessus.
cetoester qui donnera le nouveau produit estérifié. Le mécanisme est évoqué dans la figure ci-dessus.
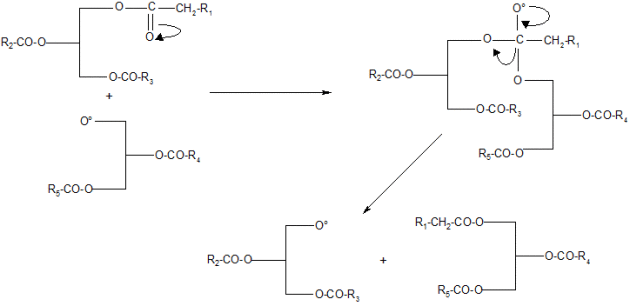
Un autre mécanisme peut être évoqué il y a addition d'un ion alkylate sur un ester carboxylique polarisé produisant un diacyglycérol intermédiaire .
Ce diacylglycérol intermédiaire attaque une nouvelle molécule de triacylglycérol pour en soustraire un acide gras et reformer un nouveau triaylglycérol et en générant un nouvel intermédiaire comme le montre la figure suivante.