La cyclomaltodextrine glucanotransférase
Définition :
La cyclomaltodextrine glucanotransférase ( EC 2 4 1 19) est une enzyme qui a la propriété de transformer les chaînes d'amidon faiblement transformées par voie enzymatique (DE de l'ordre de 5) en macrocycles: les cyclodextrines encore appelées dextrines de Schardinger.
Cette enzyme est susceptible de catalyser plusieurs types de réactions : hydrolyse, cyclisation et couplage (activité disproportionnante). C'est une enzyme qui présente beaucoup d'analogies structurales avec les
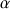 amylase (4 domaines identiques) et renferme un domaine supplémentaire. Les cyclomaltodextrine glucanotransférases sont utilisés en industries alimentaires essentiellement pour la production des cyclodextrines
amylase (4 domaines identiques) et renferme un domaine supplémentaire. Les cyclomaltodextrine glucanotransférases sont utilisés en industries alimentaires essentiellement pour la production des cyclodextrines
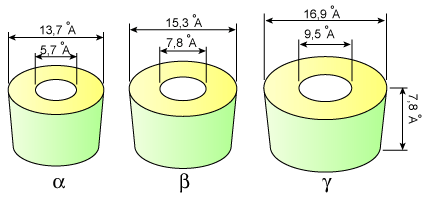
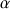 , β et γ respectivement à 6, 7 et 8 résidus de glucose enchaînés par des liaisons
, β et γ respectivement à 6, 7 et 8 résidus de glucose enchaînés par des liaisons
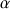 1,4 glucosidiques.
1,4 glucosidiques.
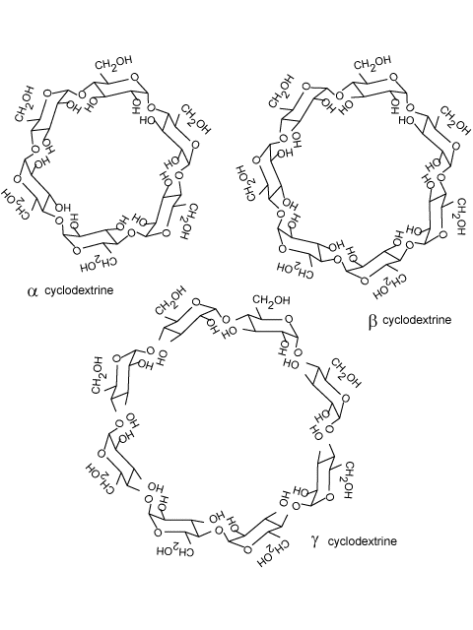
L'intérêt des cyclodextrines réside dans le fait que ces molécules possèdent une cavité de taille moyenne susceptible d'accepter des molécules en fonction de leur forme et de leur taille (phénomène d'inclusion stable). La partie interne de la cavité est hydrophobe, la partie externe est hydrophile, à la partie supérieure du torr on retrouve toutes les fonctions alcool primaire des molécules de glucose et à la partie inférieure on retrouve les fonctions alcool secondaire. Cette molécule à la particularité de pouvoir « solubiliser » les substances hydrophobes dans un milieu hydrophile. Ce phénomène d'inclusion se produit aussi avec des matières sèches. Les cyclodextrines ont la possibilité de s'associer les unes aux autres de façon à donner des ensembles soit en forme d'écaille de poisson (association tête-queue) soit sous forme de tuyau (association tête bêche).
L'inclusion permet de stabiliser ou de protéger des molécules fragiles lors de procédés agroalimentaires. Ainsi il est possible :
de stabiliser des substances volatiles (aromes), des émulsions vis-à-vis de la température
de protéger des substances vis-à-vis de l'oxydation
de protéger certains groupements fonctionnels et d'augmenter la biodisponibilité de certaines molécules
de désamériser des préparations alimentaires
d'éliminer ou de réduire fortement la teneur en caféine (thé ou café) ou du cholestérol dans les matières grasses alimentaires. Ces procédés sont fortement concurrencés par l'utilisation des fluides supercritiques.
Enfin les cyclodextrines peuvent être utilisées pour leurs propriétés chirales (fixation régio-spécifique) en chromatographie d'affinité et pour leurs propriétés à mimer les enzymes. En effet les cyclodextrines avec leur cavité peuvent être assimilées à la crevasse catalytique des enzymes et les nombreuses fonctions hydroxyles peuvent jouer le rôle des acides aminés dans le cadre d'une catalyse acide. On peut même envisager substituer ces fonctions en y greffant des acides aminés responsable d'actes catalytiques (sérine, histidine, acide glutamique ou aspartique, cystéine). Certes la réactivité de ces « néo-enzymes » est beaucoup plus faible que celle des enzymes naturelles mais quand on sait que les cyclodextrines en milieu aqueux sont stables à des températures très largement supérieures à 100°C, on peut facilement envisager le gain que cela peut représenter en stabilité et en réactivité.






