Propriétés moussantes
Définition :
Une mousse est une dispersion de bulles de gaz (azote, gaz carbonique, air) dans une phase continue (renfermant des protéines) liquide ou solide produite par agitation mécanique. Elle est caractérisée par une viscosité élevée. Il existe aussi des mousses solides pour lesquelles une phase solide ou un gel remplace le liquide une fois la dispersion réalisée. Les mousses alimentaires les plus connues sont les meringues, la crème fouettée, les soufflés, la mousse de la bière, la génoise, les pâtes levées comme la brioche, le pain, les crèmes glacées, les marshmallows...
Explication
Le volume de gaz est généralement très supérieur à celui de la phase dispersante, la taille des bulles est beaucoup plus élevée que celle des particules colloïdales. Initialement sphériques les bulles vont adopter sous la contrainte des structures plus compactes et elles deviendront polyédriques. Ce phénomène s'explique de la façon suivante : la pression est plus élevée dans une bulle de petit diamètre par rapport à une grosse bulle. La solubilité des gaz augmente avec l'augmentation de pression. Le gaz des petites bulles va se dissoudre dans le la phase continue entraînant la disparition des petites bulles. Le gaz dissous va être véhiculé par la phase continue liquide et viendra alimenter les bulles de taille supérieure qui verront leur diamètre augmenter. Les bulles vont se rapprocher, puis se déformer pour adopter une forme polyédrique. Dans ce cas de figure deux bulles sont associées par une lamelle plane qui délimite un canal de drainage. L'association de plusieurs bulles polyédriques détermine une bordure en plateau. Les différences de pression qui règne entre l'intérieur de la bulle et la lamelle liquide fait que l'eau va passer de l'intérieur de la bulle vers la lamelle effectuant ainsi un drainage et l'apparition de mousse sèche. La lamelle liquide entre les bulles peut se rompre et entraîner de ce fait une coalescence des bulles. Les mousses sont généralement moins stables que les émulsions. Les bulles ont tendance à éclater spontanément sous l'action de la trop forte tension superficielle de l'eau à moins d'ajouter un agent tensioactif qui diminuera la tension superficielle air/eau.
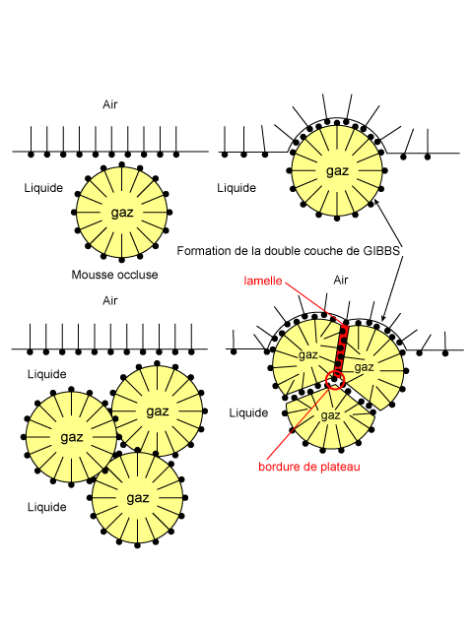
On peut fabriquer une mousse en insufflant de l'air au travers d'une structure poreuse dans une solution de protéine dont la concentration varie de 0,01 à 3% (P/V). Une mousse peut être aussi obtenue par diminution de pression d'une solution préalablement comprimée (chantilly en aérosol).
Lors de la fabrication de la mousse, on remarque dans un premier temps une augmentation de volume par intégration de gaz (expansion) et dans un deuxième temps (à l'équilibre) une diminution de volume de la phase liquide au profit de la phase mousse. Les mousses peuvent présenter des expansions de l'ordre de 10 soit l'équivalent de 1000 % si on exprime le volume de la mousse par rapport au volume d'eau compris dans la mousse. La figure ci-dessous résume ce qui se passe.
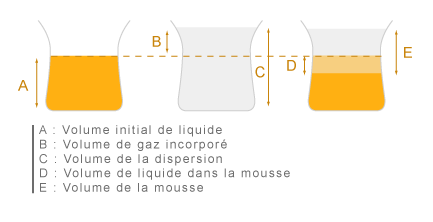
On peut déterminer et comparer les protéines quant à leurs propriétés moussantes par l'intermédiaire des paramètres suivants :
Pouvoir moussant = B/D x 100
Foisonnement = B/A x 100
Expansion = E/A x 100
Fraction volumique de gaz = B/E x 100
Les mousses qui possèdent une très grande surface interfaciale sont très facilement déstabilisées. Les protéines peuvent participer à la stabilisation des mousses.
La stabilisation est d'autant plus grande que le film protéique à l'interface gaz/liquide est plus épais, cohésif, élastique, continu et imperméable au gaz. La stabilité dépend de la conformation secondaire ou tertiaire de la protéine.
Fondamental :
Pour obtenir une bonne capacité moussante (mousse légère et expansée) il faut que la protéine soit soluble dans la phase liquide, capable de migrer rapidement dans la phase continue et pouvoir se déplisser très rapidement de façon à s'adsorber facilement au niveau de l'interface Gaz/liquide.
Il est donc très difficile de trouver une protéine qui puisse à la fois donner une mousse abondante et stable.
Les β caséines possédant une forte proportion en structure aléatoire flexible donnent des mousses abondantes à grosses bulles polyédriques instables. Le lysozyme donne une mousse moins abondante mais beaucoup plus stable (aspect crémeux avec petites bulles). Les protéines globulaires de haute masse moléculaire donnent des films épais à mousse stable car il y a la formation d'une multicouche de protéine partiellement dénaturée à l'interface. La β caséine ne donne pas de mousse (ou très peu) mais sert à la stabilisation des mousses. Dans un milieu complexe en protéine on peut remarquer des interactions entre protéines se traduisant par des phénomènes de déplacement au niveau de l'interface gaz/liquide et se répercutant sur la stabilité. Les caséines β vont déplacer très rapidement les caséines β de l'interface et vont s'y adsorber préférentiellement et de façon réversible.
Dans le cas des protéines solubles du lactosérum (lactalbumine, β lactoglobuline) le déplacement est lent, limité et non réversible. Dans certains cas il peut y avoir synergie entre les protéines soit comme l'association β lactoglobuline (couche interne) avec la к caséine (couche externe) soit encore quand des protéines acides sont associées à des protéines basiques. Dans ce dernier cas il y a aussi augmentation du pouvoir moussant dans la zone comprise entre leur pI.






