La caséine kappa
Définition :
La caséine kappa représente 8 à 15% des caséines soit 3 à 4g par litre de lait. Elle est constituée de 169 résidus d'acides aminés pour une masse moléculaire voisine de 19 kDa. Comme dans le cas des autres caséines il est possible de définir plusieurs zones. La partie N-terminal est hydrophobe, la partie C-terminal est hydrophile. L'hydrophobie moyenne d'un résidu d'acide aminé est de 5,12 kJ/mole. On caractérise dans la partie N-terminal : 15 résidus de proline et de nombreux résidus d'acides aminés hydrophobes ainsi que deux résidus de cystéine qui donneront la possibilité de contracter des ponts disulfure. Dans la partie C-terminal on met en évidence un seul résidu de phosphosérine et 6 résidus de thréonine définissant de nombreux points de glycosylation putatifs. La kappa caséine est une glycoprotéine qui renferme 5% de saccharides.
La caséine kappa précipite si la concentration en calcium dans le milieu est supérieure à 30 mM .

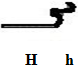
où : H représente la région hydrophobe, h représente la région hydrophile
La caséine kappa est une O-glycosyl-protéine renfermant de la N-acétylgalactosamine au niveau du point d'attache avec la thréonine, sur laquelle peut venir se brancher du galactose par des liaisons β 1,3 et de l'acide N-acétylneuraminique par une liaison
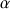 2,3 sur le résidu de galactose ou en liaison
2,3 sur le résidu de galactose ou en liaison
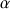 2,6 sur la N-acétylgalactosamine.
2,6 sur la N-acétylgalactosamine.
Voir tableau :
Lieu et fréquence de glycosylation de la caséine kappa
La kappa caséine renferme deux résidus de cystéine et il est possible de mettre en évidence l'existence de pont disulfure. Ces ponts disulfure sont intercaténaires et s'établissent entre les résidus de cystéine en position 11 avec une fréquence de 20%, entre les résidus de cystéine placés en position 88 avec une fréquence de 30% et entre les résidus placés en position 11 et 88 avec une fréquence de 50%. Les caséine kappa vont se polymériser avec un degré d'association qui peut atteindre 30. Cette polymérisation donne une structure hydratée lâche qui peut expliquer le pouvoir stabilisant de la caséine. Lorsque le degré de polymérisation est supérieur à 6 il n'y a plus de glycosylation.
La caséine kappa est soluble à haute force ionique même en présence de calcium, elle est très susceptible à l'action de la chymosine.






