Les différents réarrangements
Fondamental :
Toutefois, une isomérisation irréversible de la base de Schiff donne des produits plus stables. Il s'agira du réarrangement d'Amadori à partir de la condensation d'aldose avec des acides aminés pour obtenir des cétosylamines.
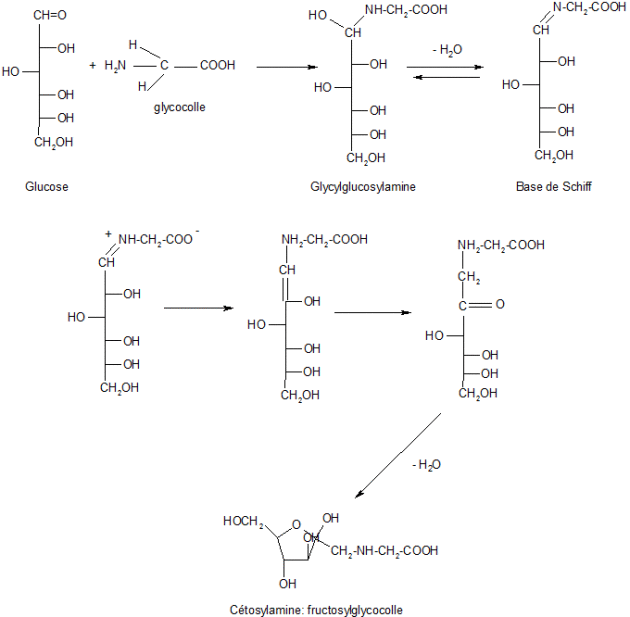
Fondamental :
Il y a possibilité d'une deuxième condensation avec le glucose pour obtenir une dicétosylamine. Dans le cas d'une condensation entre un cétose et un acide aminé on obtiendra par le mécanisme de réarrangement de Heyns-Carson une aldosylamine dans un premier temps puis une dialdosylamine.
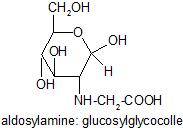
Explication
Au cours de cette étape, on a pu mettre en évidence la formation de radicaux libres. Ces produits se forment en milieu acide et apparaissent bien avant la coloration. On peut même se demander s'ils ne sont pas les véritables précurseurs des réactions de brunissement. La polymérisation de cette molécule conduit à la synthèse de dialkyldihydro pyrazine selon le schéma suivant :
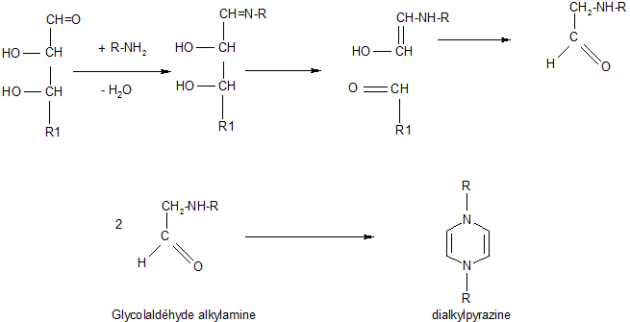
Explication
Un autre mécanisme peut être évoqué c'est celui qui aboutit à la formation de glyoxal, structure qu'on a caractérisée dans les stades précoces de la réaction.
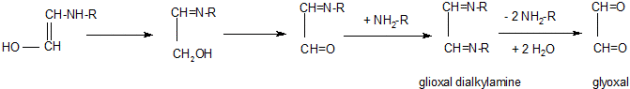
Ces molécules à petits nombre d'atomes de carbone et très réactives sont synthétisées très rapidement en présence d'alkylamines par rapport à ce qu'on obtient avec des acides aminés.






