Interaction lipide-protéine
Généralités
Les lipides qui renferment des acides gras insaturés vont pouvoir subir une attaque radicalaire puis s'oxyder et donner des radicaux très actifs comme les peroxydes, les hydroperoxydes, les oxiranes et de nouvelles fonctions carbonylées. L'autoxydation de la matière grasse découle d'un mécanisme radicalaire où l'attaque s'effectue sur le carbone placé en alpha de la double liaison (si on est en présence d'un acide gras monoinsaturé) ou sur le carbone placé entre les doubles liaisons conjuguées (quand il s'agit d'un acide gras polyinsaturé). Quand une huile de poisson est soumise à une oxydation on met en évidence la formation de propanal. Cette molécule réagit très rapidement avec la lysine du muscle pour bloquer cet acide aminé. In vitro on a pu mettre en évidence qu'un mélange de gélatine et de méthyl-linoléate soumis à un cycle de congélation-décongélation ne permettait plus de doser la lysine par la technique au dinitro-fluorobenzène. L'acide linolénique en association avec le cytochrome C, à pH 7,0 entraîne un blocage équivalent à 17,2% de la lysine et 59% pour l'histidine. On remarque que 20% des acides aminés perdus ne sont plus récupérables par une hydrolyse acide ce qui confirme que nous sommes très engagés dans la réaction de condensation.
La réaction devrait se dérouler selon la figure suivante :
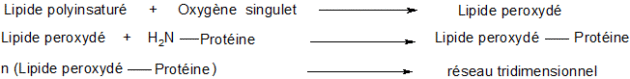
Le réseau tridimensionnel formé devient insoluble, coloré et partiellement résistant aux acides.






